烃A在一定条件下可以按下图进行转化: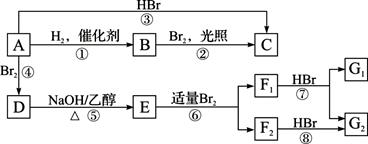
已知D为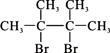 ,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2分别互为同分异构体。据此作答:
,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2分别互为同分异构体。据此作答:
(1)框图中属于取代反应的是_________(填序号);B完全燃烧后生成的CO2和水的质量比为_________。
(2)A的结构简式是_________________;G1的结构简式是____________________。
(3)写出E在一定条件下生成高聚物的化学方程式:____________________
烃A在一定条件下可以按下图进行转化:
已知D为 ,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2分别互为同分异构体。据此作答:
,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2分别互为同分异构体。据此作答:
(1)框图中属于取代反应的是_________(填序号);B完全燃烧后生成的CO2和水的质量比为_________。
(2)A的结构简式是_________________;G1的结构简式是____________________。
(3)写出E在一定条件下生成高聚物的化学方程式:____________________