“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分FeS2,其中硫元素化合价为-1价)氧化为Fe2(SO4)3,并使溶液酸性增强(生成硫酸)。
①该过程反应的化学方程式为________________________。
②人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
_____Cu2S+___Fe3++____H2O ___Cu2++Fe2++____()+SO42-
___Cu2++Fe2++____()+SO42-
 称为铁酸盐(含有FeO42-)。
称为铁酸盐(含有FeO42-)。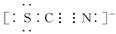
 3+氧化为FeO42-,请写出该离子反应方程式__________。
3+氧化为FeO42-,请写出该离子反应方程式__________。 物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。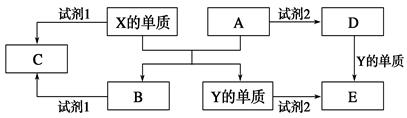
 质与试剂1反应的离子方程式是_____________。
质与试剂1反应的离子方程式是_____________。 H)SO4聚合得到的。工业上以E、稀硫酸和亚
H)SO4聚合得到的。工业上以E、稀硫酸和亚 锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。回答下列问题:
锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。回答下列问题: ______________________。
______________________。 料之一,其原理是Fe3O4+4CO3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是__________________。
料之一,其原理是Fe3O4+4CO3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是__________________。 粤公网安备 44130202000953号
粤公网安备 44130202000953号