实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.
Ⅰ.目前工业上有一种方法是用CO2与H2来生产燃料甲醇.一定条件下发生反应:
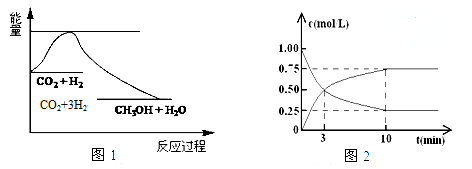
CO2(g)+3H2(g)⇌ CH3OH(g)+ H2O(g),图1表示该反应过程中能量变化:
(1)关于该反应的下列说法中,正确的是 (填字母).
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图2所示.
①从反应开始到平衡,CO2的平均反应速率v(CO2)= .
②H 2的平衡转化率为 .
③下列措施中能使化学平衡向正反应方向移动的是 (填字母).
A.升高温度 B.将CH3OH(g)及时液化抽出 C.选择高效催化剂
Ⅱ. 在一定体积的密闭容器中,进行如下化学反应CO2(g)+H2(g)  CO(g)+H2O(g),,其中化学平衡常数K和温度的关系如下表:
CO(g)+H2O(g),,其中化学平衡常数K和温度的关系如下表:
| t/℃ |
700 |
800 |
830 |
1 000 |
1 200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(1)该反应的平衡常数表达式K= 此反应为 反应(填“放热”或“吸热”)
(2)在830℃下,在10L容器中含有1molCO2、 1.2molH2、 0.75molCO、 1.5molH2O,则此时反应v(N2)正________ v(N2)逆(填“>”、“<”、“=”),对此反应状态的描述正确的为 (填下列序号)
A.恰好处于平衡状态 B.向正反应方向进行 C.向逆反应方向进行
 [CuCl4]2-+4H2O
[CuCl4]2-+4H2O 粤公网安备 44130202000953号
粤公网安备 44130202000953号