25℃时,几种酸的电离平衡常数如下:
| 化学式 |
CH3COOH |
H2CO3 |
HClO |
| 电离平衡常数 |
1.8×10-5 |
Ka1= 4.3×10-7 Ka2= 5.6×10-11 |
3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:a.Na2CO3溶液,b.NaClO溶液,c.CH3COONa溶液d.NaHCO3溶液;pH由大到小的顺序是:_______________________(填编号)。
(2)常温下0.1mol/L的CH3COOH溶液加水稀释过程中,下列各项的数值一定变小的是:__________。
A. c(H+) B. c(H+)/c(CH3COOH) C. c(H+)·c(OH-) D. c(OH-)/c(H+)
(3)体积均为10mL pH均为2的CH3COOH溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:稀释后, HX溶液中水电离出来的c(H+)_____(填“大于”、“等于”或“小于”)
CH3COOH溶液中水电离出来的c(H+),理由是__________________________________。

(4)25℃时,测得CH3COOH与CH3COONa的混合溶液PH=6,则溶液中c(CH3COO-)- c(Na+)=_______________________。(填准确数值)
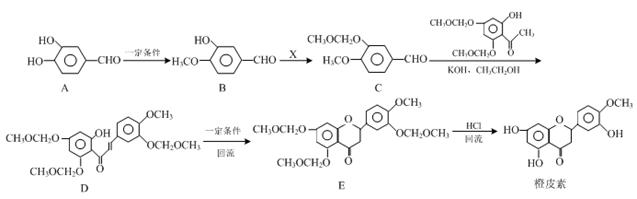
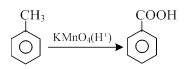
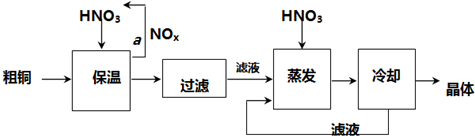
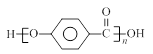 的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。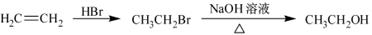

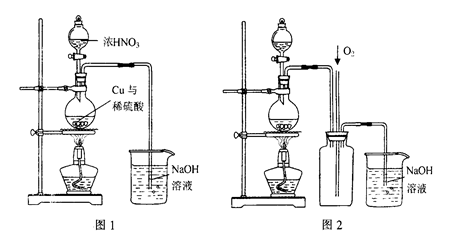

 2NH3(g),则在电解法合成氨的过程中,应将H2不断地通入_________极(填“阴”或“阳”;向另一电极通入N2,该电极的反应式为__________________________。
2NH3(g),则在电解法合成氨的过程中,应将H2不断地通入_________极(填“阴”或“阳”;向另一电极通入N2,该电极的反应式为__________________________。 2NH3(g)△H=-93.0kJ/mol。某小组进行工业合成氨的模拟研究,在1L密闭容器中,分别加入0.1mol N2和0.3mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
2NH3(g)△H=-93.0kJ/mol。某小组进行工业合成氨的模拟研究,在1L密闭容器中,分别加入0.1mol N2和0.3mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
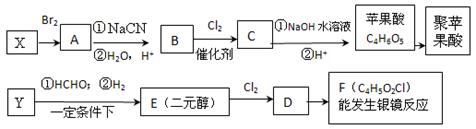
 RC≡C-CH2OH;
RC≡C-CH2OH; RCH2COOH;
RCH2COOH;
 粤公网安备 44130202000953号
粤公网安备 44130202000953号