煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:

一定温度下,在一个容积固定的密闭容器中,发生上述反应,下列不能判断该反应达到化学平衡状态的是___________________(填字母)。
a.容器中的压强不变
b.1 mol H-H键断裂的同时断裂2 mol H-O键
c. 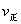 (CO)=
(CO)= (H2O)
(H2O)
d.c (CO) =" c" (H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应
CO(g)+H2O(g) ⇌CO2 (g)+H2 (g) ,得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
| H2O |
CO |
H2 |
CO2 |
|||
| 1 |
650 |
2 |
4 |
1.6 |
1.6 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
0.4 |
3 |
| 3 |
900 |
a |
b |
c |
d |
t |
①该反应的逆反应为____________(填“吸”或“放”)热反应
②若实验3要达到与实验2中各物质的质量分数分别相等,且t<3min,则a、b应满足的关系是______________(用含a、b的数学式表示)。
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:
CO2 (g)+3H2 (g)  CH3OH(g)+H2O(g)右图表示该反应进行过程中能量(单位为kJ・mol。)的变化。
CH3OH(g)+H2O(g)右图表示该反应进行过程中能量(单位为kJ・mol。)的变化。

①在体积为1 L的恒容密闭容器中,充入l molCO2和3molH2,下列措施中能使 c (CH3OH)增大的是_______(填字母)
a.升高温度
b.充入He (g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入l mol CO2和3 molH2
②当反应达到平衡时不断改变条件(但不改变各组分物质的量和状态)反应速率随时间的变化如右图:其中表示平衡混合物中CH3OH含量最高的一段时间是_______________;如t0~t1平衡常数为K1, t2~t3平衡常数为K2 ,则K1_______________K2(填“大于”、“等于”或“小于”)。


 5NaCl+NaClO3+3H2O,请推测在加热NaClO溶液时发生反应的化学方程式:______________________________。
5NaCl+NaClO3+3H2O,请推测在加热NaClO溶液时发生反应的化学方程式:______________________________。




 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
 粤公网安备 44130202000953号
粤公网安备 44130202000953号