单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备,其中X为Z的氧化物.Y为氢化物,分子结构与甲烷相似,回答下列问题;
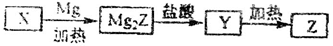
(1)能与X发生化学反应的酸是_______(写名称);由X制备Mg2Z的化学方程式为___ __。
(2)由Mg2Z生成Y的化学反应方程式为___________________,Y分子的电子式为________________
(3)Z、X中化学键的类型都是_________________。
单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备,其中X为Z的氧化物.Y为氢化物,分子结构与甲烷相似,回答下列问题;
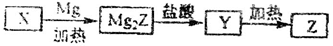
(1)能与X发生化学反应的酸是_______(写名称);由X制备Mg2Z的化学方程式为___ __。
(2)由Mg2Z生成Y的化学反应方程式为___________________,Y分子的电子式为________________
(3)Z、X中化学键的类型都是_________________。