下图所示装置是实验室常用的气体制取装置。据图回答下列问题: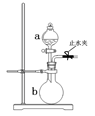
(1)仪器a的名称____________,检查装置气密性操作为____________________。
(2)若实验室制取C2H2,a中盛放的药品为__________________;若制取氨气且a中盛放的药品为浓氨水,则b中盛放的固体药品为____________________;若需同时制取NH3和O2用于进行NH3的催化氧化实验,则b中所放的固体药品为________________。
下图所示装置是实验室常用的气体制取装置。据图回答下列问题:
(1)仪器a的名称____________,检查装置气密性操作为____________________。
(2)若实验室制取C2H2,a中盛放的药品为__________________;若制取氨气且a中盛放的药品为浓氨水,则b中盛放的固体药品为____________________;若需同时制取NH3和O2用于进行NH3的催化氧化实验,则b中所放的固体药品为________________。