黑色粉末A,黄色粉末B,它们都是单质,按下图进行实验:
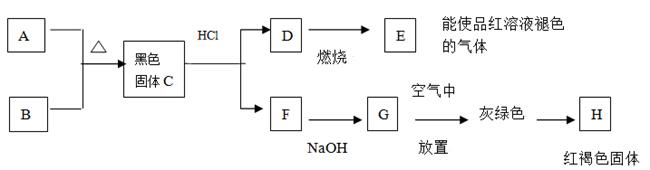
(1) 试根据上述反应现象推断以下物质的化学式:
A D E H
 (2)写出C+盐酸 D+F的离子方程式:
(2)写出C+盐酸 D+F的离子方程式:
(3)写出D E的化学方程式:
E的化学方程式:
(4)写出G H的化学方程式:
H的化学方程式:
黑色粉末A,黄色粉末B,它们都是单质,按下图进行实验:

(1) 试根据上述反应现象推断以下物质的化学式:
A D E H
 (2)写出C+盐酸 D+F的离子方程式:
(2)写出C+盐酸 D+F的离子方程式:
(3)写出D E的化学方程式:
E的化学方程式:
(4)写出G H的化学方程式:
H的化学方程式: