一密闭体系中发生下列反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,下图是某一时间段中反应速率与反应时间的曲线关系图,回答下列问题:
2NH3(g) ΔH<0,下图是某一时间段中反应速率与反应时间的曲线关系图,回答下列问题: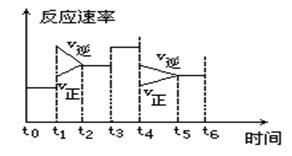
(1)处于平衡状态的时间段是_________________
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化?________________________。
(3)下列各时间段内,氨的百分含量最高的是
| A.t0~t1 | B.t2~t3 | C.t3~t4 | D.t5~t6 |
一密闭体系中发生下列反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,下图是某一时间段中反应速率与反应时间的曲线关系图,回答下列问题:
2NH3(g) ΔH<0,下图是某一时间段中反应速率与反应时间的曲线关系图,回答下列问题:
(1)处于平衡状态的时间段是_________________
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化?________________________。
(3)下列各时间段内,氨的百分含量最高的是
| A.t0~t1 | B.t2~t3 | C.t3~t4 | D.t5~t6 |