某化学探究小组拟用废铜屑制取Cu(NO3)2并探究其化学性质。
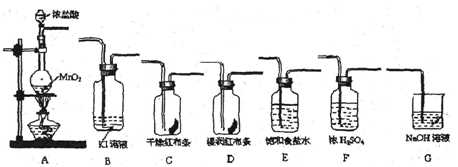
I、如右图所示,用浓HNO3和过量的废铜屑充分反应制硝酸铜溶液。

(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤依次是:蒸发浓缩、 、过滤、 、烘干。
③你认为此装置是否合理,并说明原因 。
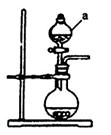
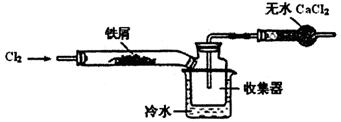
Ⅱ、为了探究Cu(NO3)2热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)

(3)往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;在集气瓶中收集到无色气体。由此判断Cu(NO3)2受热分解的化学方程式为 。
Ⅲ、利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。下表是化学探究小组的实验记录,据此回答相关问题:
| 实验序号 |
1 |
2 |
3 |
4 |
| 温度/℃ |
35 |
50 |
70 |
95 |
| 样品颜色 |
深蓝色 |
深蓝色 |
浅绿色 |
暗蓝色 |
(4)95℃时,制得的样品颜色发暗的可能原因是: 。
(5)70℃时,实验得到3.82 g样品,取此样品加热至分解完全(杂质不反应),得到3.20 g固体,此样品中碱式碳酸铜的质量分数是 。
 NaClO3+3H2
NaClO3+3H2 ,2NaClO3+4HCl=2C1O2
,2NaClO3+4HCl=2C1O2
 粤公网安备 44130202000953号
粤公网安备 44130202000953号