按要求回答下列问题
(1)、4g CO在氧气中燃烧生成CO2,放出 9. 6kJ热量,写出CO燃烧的热化学方程式。_____________________________
(2)、已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为________________________
(3)、已知碳的燃烧热ΔH1=" a" kJ·mol-1 S(s)+2K(s)==K2S(s) ΔH2=" b" kJ·mol-1
2K(s)+N2(g)+3O2(g)==2KNO3(s) ΔH3=" c" kJ·mol-1
则S(s)+2KNO3(s)+3C(s)==K2S(s)+N2(g)+3CO2(g) ΔH=
(4)、已知:C(s)+O2(g)=CO2(g) ΔH="-437.3" kJ·mol一1
H2(g)+1/2O2(g)=H2O(g) ΔH="-285.8" kJ·mol一1
CO(g)+1/2O2(g)=CO2(g) ΔH="-283.0" kJ·mol一1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式
计算10m3(标况)水煤气完全燃烧放出的热量为 kJ(结果保留到小数点后一位)。
 SiC+2CO↑在这个氧化还原反应中,氧化剂和还原剂的物质的量之比是________。
SiC+2CO↑在这个氧化还原反应中,氧化剂和还原剂的物质的量之比是________。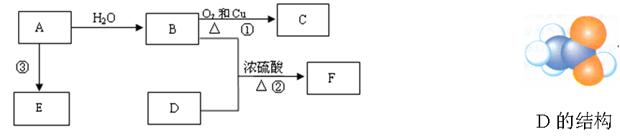
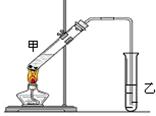
 ;
;
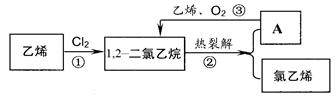
 的中间体——草酸二乙酯(C2H5OOCCOOC2H5)(用反应流程图表示,并注明反应条件)。
的中间体——草酸二乙酯(C2H5OOCCOOC2H5)(用反应流程图表示,并注明反应条件)。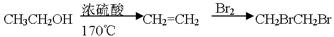
 C2H5O-NO2+H2O
C2H5O-NO2+H2O 分子式为________________。
分子式为________________。 能的结构简式:________________________________________________。
能的结构简式:________________________________________________。 粤公网安备 44130202000953号
粤公网安备 44130202000953号