环己烯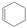 又名四氢化苯,回答下列问题
又名四氢化苯,回答下列问题
(1) 推测环己烯_______(能、不能)使酸性高锰酸钾溶液褪色。
(2) 环己烯属于__________
| A.乙烯的同系物 |
B.苯的同系物 |
| C.碳氢化合物 |
D.己烯的同分异构体 |
E、芳香烃
(3) 将环己烯与溴的四氯化碳溶液混合充分震荡后,溴的四氯化碳溶液褪色,
写出反应的化学方程式___________________,反应类型为___________
(4) 已知环己烯与水在一定条件下可以发生加成反应生成A,A中含氧官能团名称为____________。