卤族元素是典型的非金属元素,卤素单质及其化合物在工农业生产和生活中都有重要的用途。
(1)同主族元素的电负性大小存在一定的规律,卤族元素(F、Cl、Br、I)中,电负性最大的是 。
(2)不同卤素原子之间可形成卤素互化物,如IBr、BrI3、BrF5、IF,等。卤素互化物中的化学键类型是 (填标号)。
| A.极性键 | B.非极性键 | C.离子键 | D.σ键 |
(3)BeCl2的分子空间构型为__________;BF3分子中B-F键的键角为_____________。
(4)CCl4分子中的C原子和NF3分子中的N原子的杂化方式是否相同? 。如果相同,则其杂化方式为 ;如果不相同,则其杂化方式分别为 。(后两个空只能填一个,若两空都填,则不给分)
(5)HF的相对分子质量小于HC1,但其沸点却高于HC1,其原因是________________
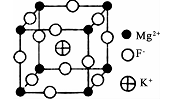
(6)由F、Mg、K三种元素形成的某种晶体的晶胞结构如下图所示,晶胞边长为anm,该晶体的化学式为_________________________;列式计算该晶体的密度(g.cm-3)


 粤公网安备 44130202000953号
粤公网安备 44130202000953号