核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:
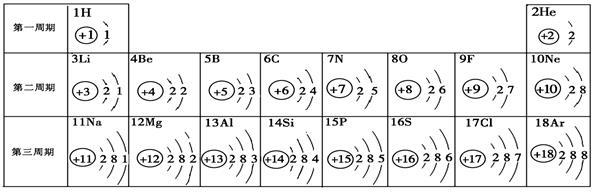
(1)分析其规律可知,每一周期元素原子的 相同。
(2)表中9号和17号元素最外层电子数相同,都易 (填“得到”或“失去”)电子。
(3)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以稀有气体结尾。
核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:

(1)分析其规律可知,每一周期元素原子的 相同。
(2)表中9号和17号元素最外层电子数相同,都易 (填“得到”或“失去”)电子。
(3)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以稀有气体结尾。