已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
| 醋酸 |
碳酸 |
亚硫酸 |
| Ka= 1.75×10-5 |
Ka1= 4.30×10-7 Ka2 = 5.61×10-11 |
Ka1= 1.54×10-2 Ka2 = 1.02×10-7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = 。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱: > > 。
(3)下图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化
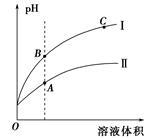
①图像中,曲线I表示的酸是 (填化学式)。
②A、B、C三点中,水的电离程度最大的是 (填字母)。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号