(8分)某同学利用如图所示的装置进行有关实验。其中气体A的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题:
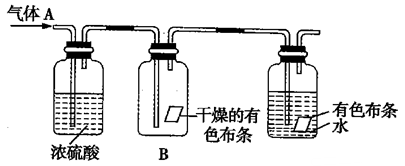
(1)该实验的主要目的是研究干燥的氯气是否具有 作用。
(2)浓硫酸的作用是
(3)实验过程中观察到B瓶中干燥的有色布条 (填“A.退”或“B.不退”)色。
(4)在该实验中,装置存在缺陷,还应加盛有 的装置。
(8分)某同学利用如图所示的装置进行有关实验。其中气体A的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题:

(1)该实验的主要目的是研究干燥的氯气是否具有 作用。
(2)浓硫酸的作用是
(3)实验过程中观察到B瓶中干燥的有色布条 (填“A.退”或“B.不退”)色。
(4)在该实验中,装置存在缺陷,还应加盛有 的装置。