如图是甲、乙、丙(均不含结晶水)三种物质的溶解度曲线,请据图回答下列问题.
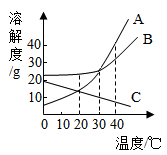
(1)在40℃时,甲、乙、丙三种物质的溶解度由大到小的关系是 (物质间用“>”连接);
(2)将30℃的三种物质的饱和溶液冷却到20℃后,所得溶液中溶质的质量分数由小到大的关系是:
(物质间用“<”连接);
(3)现有一定质量的B溶液,将该溶液在50℃下恒温蒸发10克水后析出了2克B晶体,再恒温蒸发5克水后,又析出了2克B晶体,则B物质在50℃时的溶解度是: .
如图是甲、乙、丙(均不含结晶水)三种物质的溶解度曲线,请据图回答下列问题.

(1)在40℃时,甲、乙、丙三种物质的溶解度由大到小的关系是 (物质间用“>”连接);
(2)将30℃的三种物质的饱和溶液冷却到20℃后,所得溶液中溶质的质量分数由小到大的关系是:
(物质间用“<”连接);
(3)现有一定质量的B溶液,将该溶液在50℃下恒温蒸发10克水后析出了2克B晶体,再恒温蒸发5克水后,又析出了2克B晶体,则B物质在50℃时的溶解度是: .