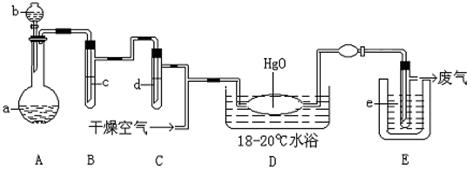
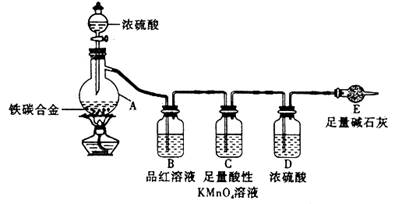
某化学小组用下列装置制取收集纯净的氯气,并研究其性质。请回答下列问题。

(1)装置甲中仪器A的名称是________,丙中应装的溶液是 ,甲装置中发生反应的离子方程
式为 。制取收集纯净氯气的装置接口连接顺序是a→ …→g(补充完整) 。
(2)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
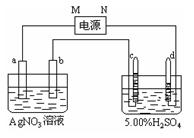
I方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
Ⅱ方案:采用酸碱中和滴定法测定。
Ⅲ方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
继而进行下列判断和实验:
①判定I方案不可行,理由是__________________;
②进行Ⅱ方案实验:准确量取残余清液稀释一定倍数后作为试样。
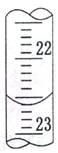
a.量取试样20.00mL于锥形瓶中,若锥形瓶中存有少量水,对实验结果是否有影响? (填“是”或“无”)。用0.10 mol•L-1 NaOH标准溶液滴定,消耗NaOH标准溶液的体积如右图所示 ,其读数为 mL.
b.平行滴定后获得实验结果
③判断Ⅲ方案的实验结果_______(填“偏大”、“偏小”或“准确”)。[已知:Ksp(CaCO3)=2.8×10-9、Ksp(MnCO3)=2.3×10-11
(3)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂。



 。
。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号