如图所示:A、B、C、D是初中化学中常见的不同类别的物质,已知A、B是空气中的两种气体,“ ”表示两种物质在一定条件下可相互转变。依据给出的信息推断并回答下列问题:
”表示两种物质在一定条件下可相互转变。依据给出的信息推断并回答下列问题:
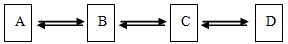
(1)B转化为A的过程叫 ;
(2)B物质的一种用途是 ;
(3)C物质所属的类别是 ;
(4)D转化为C的反应方程式是 。
如图所示:A、B、C、D是初中化学中常见的不同类别的物质,已知A、B是空气中的两种气体,“ ”表示两种物质在一定条件下可相互转变。依据给出的信息推断并回答下列问题:
”表示两种物质在一定条件下可相互转变。依据给出的信息推断并回答下列问题:

(1)B转化为A的过程叫 ;
(2)B物质的一种用途是 ;
(3)C物质所属的类别是 ;
(4)D转化为C的反应方程式是 。