根据下列装置图,回答有关问题:
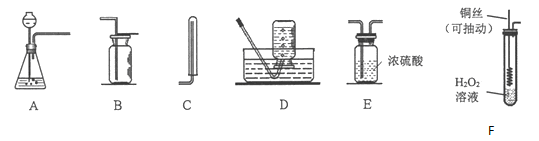
(1)实验室用过氧化氢制取氧气的化学方程式为
(2)实验室常用锌粒和稀硫酸反应制取氢气,有关反应的化学方程式为
(3)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂.现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经过
①铜丝绕成螺旋状的作用是
②与装置A比较,改进后装置的优点是
根据下列装置图,回答有关问题:

(1)实验室用过氧化氢制取氧气的化学方程式为
(2)实验室常用锌粒和稀硫酸反应制取氢气,有关反应的化学方程式为
(3)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂.现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经过
①铜丝绕成螺旋状的作用是
②与装置A比较,改进后装置的优点是