下图中X是一种具有水果香味的合成香料,A是直链有机物,E与FeCl3溶液作用显紫色。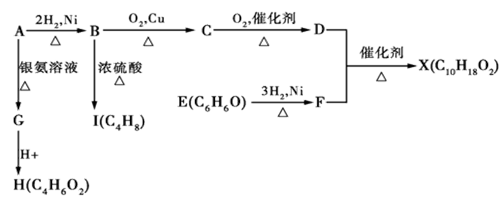
请根据上述信息回答:
(1)H中含氧官能团的名称是________,B→I的反应类型为______________。
(2)只用一种试剂鉴别D、E、H,该试剂是_________________。
(3)H与J互为同分异构体,J在酸性条件下水解有乙酸生成,J的结构简式为_____________。
(4)D和F反应生成X的化学方程式为________________。
下图中X是一种具有水果香味的合成香料,A是直链有机物,E与FeCl3溶液作用显紫色。
请根据上述信息回答:
(1)H中含氧官能团的名称是________,B→I的反应类型为______________。
(2)只用一种试剂鉴别D、E、H,该试剂是_________________。
(3)H与J互为同分异构体,J在酸性条件下水解有乙酸生成,J的结构简式为_____________。
(4)D和F反应生成X的化学方程式为________________。