地球是一颗美丽的蓝色星球,海水占了全球水资源的97
.海水资源的开发和利用具有非常广阔的前景.
(1)海水中含有大量的
,可用于制备钠及其化合物,其流程如图:
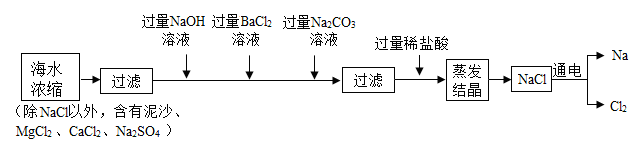
①加入过量
溶液目的是除去
和
②提纯过程中使用了过滤和蒸发操作,实验室过滤和蒸发操作均使用到的玻璃仪器是
③流程图中制备金属钠的化学方程式为
(2)工业上利用电解饱和食盐水的方法制备
,并同时获得两种单质.补充并配平化学方程式:
□
+□
□
(3)刘廷在实验室找到一瓶长期放置的
溶液,欲对其成分进行实验探究.
【查阅资料】
Ⅰ.
与
分两步反应:
Ⅱ. 与 反应方程式为:
Ⅲ.物质的溶解性:
|
|
|
|
|
|
|
不溶 |
溶 |
溶 |
溶液的酸碱性:
溶液呈中性
【提出猜想】刘廷根据资料中的Ⅰ、Ⅱ对其成分提出了5种合理猜想,请将猜想补充完整
猜想1:只有
猜想2:
猜想3:只有
猜想4:
猜想5:只有
【实验验证】
| 步骤 |
操作 |
现象 |
结论 |
| 步骤1 |
取该
溶液,加入过量
溶液 |
产生白色沉淀 |
证明猜想1、5不成立, |
| 步骤2 |
取步骤1中上层清液,滴加 |
无气泡产生 |
证明原溶液不含 |
| 步骤3 |
另取步骤1中上层清液,滴加 |
溶液未变红 |
证明原溶液不含 |
【实验结论】
通过以上实验操作得出结论:猜想



 粤公网安备 44130202000953号
粤公网安备 44130202000953号