已知氯酸钾和亚硫酸氢钠发生氧化还原反应时,生成-1价的氯和+6价的硫的化合物,反应速率v和反应时间t的关系如图所示。已知这个反应的反应速率随溶液中氢离子浓度增大而加快,试解释: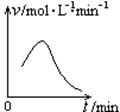
(1)反应开始后,反应速率加快的原因是______________________。
(2)反应后期,反应速率下降的原因是________________________。
已知氯酸钾和亚硫酸氢钠发生氧化还原反应时,生成-1价的氯和+6价的硫的化合物,反应速率v和反应时间t的关系如图所示。已知这个反应的反应速率随溶液中氢离子浓度增大而加快,试解释:
(1)反应开始后,反应速率加快的原因是______________________。
(2)反应后期,反应速率下降的原因是________________________。