"铁、锌、铜、镁、铝"是生活中常见的金属。请根据所学知识回答下列问题:
(1)铝块能制成铝箔是利用了铝的
(2)黄铜是铜锌合金,其硬度比纯铜
(3)将一定质量的锌粒投入含有
和
的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有
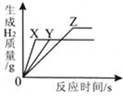
(4)将等质量的镁、铁、锌三种金属分别放入三份溶质质量分数相等的稀盐酸 中。生成氢气的质量与反应时间的关系如图所示。金属
是
"铁、锌、铜、镁、铝"是生活中常见的金属。请根据所学知识回答下列问题:
(1)铝块能制成铝箔是利用了铝的
(2)黄铜是铜锌合金,其硬度比纯铜
(3)将一定质量的锌粒投入含有
和
的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有
(4)将等质量的镁、铁、锌三种金属分别放入三份溶质质量分数相等的稀盐酸 中。生成氢气的质量与反应时间的关系如图所示。金属
是
