某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究。
【查阅资料】SO2Cl2名称是氯化硫酰,常温下是无色液体,极易水解,遇潮湿空气会产生白雾。
【讨论】(1)SO2Cl2中S元素的化合价是 。
(2)实验中制取的SO2和Cl2在混合前都必须提纯和干燥。
【实验探究】(1)实验中制得了干燥纯净的SO2和Cl2。
(2)按下图收集满Cl2后,再通入SO2,集气瓶中立即有无色液体产生,充分反应后,将无色液体和剩余气体分离,分别对无色液体和剩余气体进行如下探究。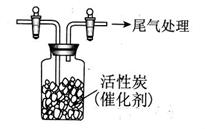
Ⅰ.探究反应产物。
向所得无色液体中加入水,立即产生白雾,振荡,静置,得无色溶液。经检验:该无色溶液中的阴离子(除OH-外)只有SO42-、Cl-。证明无色液体为SO2Cl2。
(1)SO2Cl2与水反应的化学方程式是 。
(2)验证无色溶液中含有Cl-的方法是 。
Ⅱ.探究反应进行的程度。
用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再加入BaCl2溶液,立即产生白色沉淀。
证明SO2与Cl2的反应是可逆反应。
阐述证明SO2与Cl2是可逆反应的理由 。
【质疑】有同学提出:选修四教材习题中介绍SOCl2(亚硫酰氯)常温下是无色液体,极易水解,遇潮湿空气也会产生白雾。SO2与Cl2反应若还能生成SOCl2则无法证明生成的是SO2Cl2。
SO2Cl2与水反应的化学方程式是 。
小组讨论后认为不会生成SOCl2,理由是 。
 断滴定终点。实验步骤如下:
断滴定终点。实验步骤如下: 如果锥形瓶中含有少量蒸馏水,是否会影响测量结果(填“是”、“否”、“不能确定”),
如果锥形瓶中含有少量蒸馏水,是否会影响测量结果(填“是”、“否”、“不能确定”), 曲线图。
曲线图。
 、“不正确”)
、“不正确”)
 是________。
是________。 和C
和C H
H 的比例关系,设计实验如下图所示:
的比例关系,设计实验如下图所示:
 D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等……
D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…… l
l 是烷烃裂解的催化剂;G后面装置已省略。
是烷烃裂解的催化剂;G后面装置已省略。



 溶液的棉花。给试管加热,观察现象。当反应一段时间以后,停止加热。回答下列问题:
溶液的棉花。给试管加热,观察现象。当反应一段时间以后,停止加热。回答下列问题: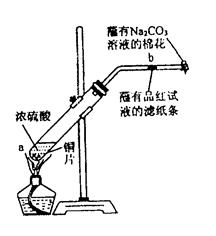
 处滤纸条的变化为。待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为。
处滤纸条的变化为。待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为。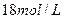 ,铜片是过量的,加热使之反应,当被还原的硫酸为
,铜片是过量的,加热使之反应,当被还原的硫酸为 。则浓硫酸的实际体积(填写“大于”、“等于”或“小于”)
。则浓硫酸的实际体积(填写“大于”、“等于”或“小于”) 。
。 粤公网安备 44130202000953号
粤公网安备 44130202000953号