一学习小组利用下图所示装置,对某含少量Fe的废铜屑进行铜含量的测定,并探究利用其制备硫酸铜溶液。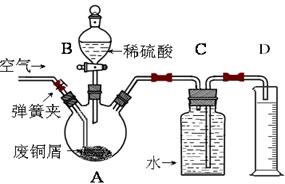
(1)向A中加入10g废铜屑样品,关闭弹簧夹,打开B活塞向A注入足量稀硫酸后关闭。此时装置C中发生的现象是 。
(2)反应进行到A中不再产生气泡时,拆除C、D装置后,为了使A中固体全部消失,①接下来的操作是:______________________________。
②该过程中发生反应的离子方程式是 ;
③为使A中固体加快溶解速率,以下方法运用合理的是 。
a. 对A装置加热
b. 向A内加入少量Fe2O3
c. 向A内加入少量CuO
d. 增大空气通入量
e. 向A内加入少量FeSO4
f. 向A内加入少量H2O
(3)待A中固体全部溶解后,再继续通入一段时间空气后,关闭弹簧夹,停止通入空气。将A中溶液倒入烧杯内,加入Cu2(OH)2CO3将其调节至pH=4时,溶液中铁被完全沉淀,过滤后即得红褐色沉淀与硫酸铜溶液,此过程离子反应方程式是 __________。
(4)有同学认为,可以不用测量气体法计算废铜屑中铜的质量百分含量,其具体操作步骤可续写为:
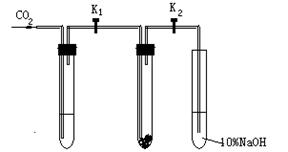
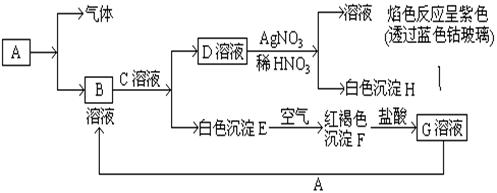


 混合液的颜色逐渐变黑,请用简要文字和化学方程式说明原因__________________________________________________________________。
混合液的颜色逐渐变黑,请用简要文字和化学方程式说明原因__________________________________________________________________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号