电解工作原理的实际应用非常广泛。
(1)电解精炼银时,阴极反应式为____________________________________。
(2)工业上为了处理含有Cr2O72-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是________
A.阳极反应:Fe-2e-===Fe2+
B.阴极反应:2H++2e-===H2↑
C.在电解过程中工业废水由酸性变为碱性
D.可以将铁电极改为石墨电极
(3)某同学设计了如下图装置进行以下电化学实验。
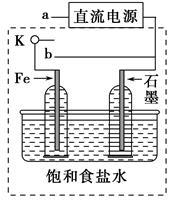
①当开关K与a连接时,两极均有气泡产生,则阴极为_______________极。
②一段时间后,使开关K与a断开、与b连接时,虚线框内的装置可称为__________。
请写出此时Fe电极上的电极反应式__________________。
(4)1 L某溶液中含有的离子如下表:
离子
|
Cu2+
|
Al3+
|
NO3-
|
Cl-
|
物质的量浓度( mol·L-1)
|
1
|
1
|
a
|
1
|
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是________
A.电解后溶液呈酸性
B.a=3
C.阳极生成1.5 mol Cl2
D.阴极析出的金属是铜与铝