(共4分)
(1)25℃时,水的离子积常数KW为1.0×10—14;在pH=2的稀硫酸中,c(OH—) = ;若升高温度,会使KW 数值 (填“增大”、“减小”或“不变”)。
(2)在醋酸水溶液中存在平衡CH3COOH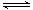 CH3COO—+H+。若分别改变下列条件:①加水稀释 ②加热 ③加少量固体醋酸钠,其中能使醋酸电离程度增大的是 ,能使溶液pH增大的是 (填序号)。
CH3COO—+H+。若分别改变下列条件:①加水稀释 ②加热 ③加少量固体醋酸钠,其中能使醋酸电离程度增大的是 ,能使溶液pH增大的是 (填序号)。
(共4分)
(1)25℃时,水的离子积常数KW为1.0×10—14;在pH=2的稀硫酸中,c(OH—) = ;若升高温度,会使KW 数值 (填“增大”、“减小”或“不变”)。
(2)在醋酸水溶液中存在平衡CH3COOH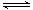 CH3COO—+H+。若分别改变下列条件:①加水稀释 ②加热 ③加少量固体醋酸钠,其中能使醋酸电离程度增大的是 ,能使溶液pH增大的是 (填序号)。
CH3COO—+H+。若分别改变下列条件:①加水稀释 ②加热 ③加少量固体醋酸钠,其中能使醋酸电离程度增大的是 ,能使溶液pH增大的是 (填序号)。