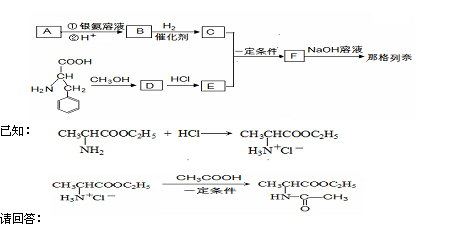
那格列奈是一种新型的餐时血糖调节剂,适用于2型糖尿病。其合成路线如下:
(1)有机物A蒸气密度是相同状态下氢气密度的74倍,A分子中碳元素的质量分数是氢元
素质量分数的10倍,A的1个分子中含有1个氧原子, A中含氧官能团的名称为;
A的分子式为。
(2)A的结构满足以下条件:
① 含有苯环,苯环上有两个取代基
② 苯环上的一溴取代物只有两种
③ 取代基上有三种不同的氢
写出A的结构简式:____________________________________________________________
(3)写出流程中制取D的化学方程式;
_____________________________________________________________________________
(4)由F制取那格列奈的反应类型是____________________
(5)(5)1 mol B与3 mol H2加成得到C,写出由C和E制取F的化学方程式:
___________________________________________________________________________、