【化学—有机化学基础】PPMB(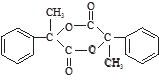 )是一种重要的化工原料,在药物、新材料等方面有重要的应用,合成该有机物的一种路线如下:
)是一种重要的化工原料,在药物、新材料等方面有重要的应用,合成该有机物的一种路线如下:
已知:
(1)试剂X为____________________;E中含氧官能团名称为__________。
(2)遇氯化铁溶液显紫色且苯环上有两个取代基的D的同分异构体有________种。
(3)E在一定条件下可以生成高聚物F,F的结构简式为___________。
(4)PPMB与足量氢氧化钠的水溶液共热的化学方程式为__________________。
【化学—有机化学基础】PPMB( )是一种重要的化工原料,在药物、新材料等方面有重要的应用,合成该有机物的一种路线如下:
)是一种重要的化工原料,在药物、新材料等方面有重要的应用,合成该有机物的一种路线如下:
已知:
(1)试剂X为____________________;E中含氧官能团名称为__________。
(2)遇氯化铁溶液显紫色且苯环上有两个取代基的D的同分异构体有________种。
(3)E在一定条件下可以生成高聚物F,F的结构简式为___________。
(4)PPMB与足量氢氧化钠的水溶液共热的化学方程式为__________________。