【化学—选修3物质结构与性质】已知:碳、氮、氢、氧四种元素可形成多种化合物,且有非常重要的用途。
(1)C、N、H电负性的大小顺序为 。
(2)甲烷与二氧化氮可发生如下反应:CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g) ,若反应中有2mol C-H键断裂,则形成的π键共有 mol。
(3)F2与NH3在一定条件下可形成NF3,NF3分子的空间构型为 形 。
(4)现已合成出一种硬度比金刚石还大的晶体氮化碳,其化学式为 。其硬度比金刚石大的主要原因是 。
(5)配合物Y的结构如图所示,Y中含有 (填序号)。
A.非极性共价键
B.配位键
C.极性键
D.氢键
E.金属键
Y中碳原子的杂化方式有 。
写出镍(Ni)原子的价电子排布式 。
(6)氨气与铁在一定条件下发生置换反应,一种产物的晶胞结构如下图所示,若该立方体晶胞的棱长为a pm,则该晶体的密度为 g/cm3(NA为阿佛加德罗常数的值)。


 HClO+ OH-
HClO+ OH-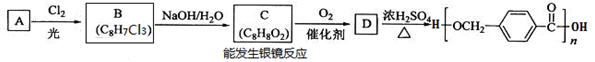
 粤公网安备 44130202000953号
粤公网安备 44130202000953号