锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2, 可通过下列反应制备: 2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O。请回答下列问题。
(1)上述方程式中涉及到的N、 O元素电负性由小到大的顺序是 。
(2)基态S的价电子排布式为 。与Cu同周期且最外层电子数相等的元素还有 (填元素符号)。
(3)PO43-的空间构型是 , 其中P原子的杂化方式为 。
(4)在硫酸铜溶液中加入过量的KSCN溶液, 生成配合物[Cu(CN)4]2-则1molCN-中含有的π键的数目为 。
(5)铜晶体为面心立方最密集堆积, 铜的原子半径为127.8pm, 列式计算晶体铜的密度 g/cm3。
(6)下表列出了含氧酸酸性强弱与非羟基氧原子数的关系。
由此可得出的判断含氧酸强弱的一条经验规律是 。亚磷酸 (H3PO3) 也是中强酸,它的结构式为 。亚磷酸与过量的氢氧化钠溶液反应的化学方程式为 。
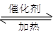 7N2+12 H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是L。
7N2+12 H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是L。 2SO3(g) ΔH="-196.6" kJ·mol-1
2SO3(g) ΔH="-196.6" kJ·mol-1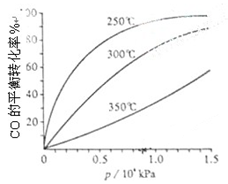
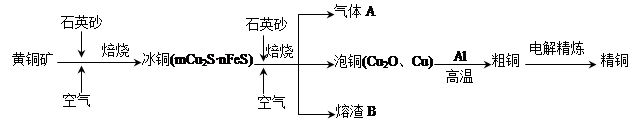
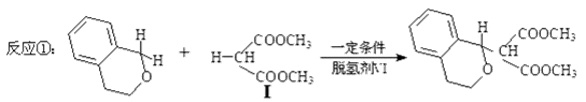
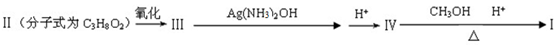
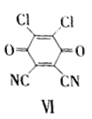
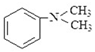 与1分子
与1分子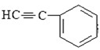 在一定条件下可发生类似反应①的反应,其产物分子的结构简式为____________;1mol该产物最多可与______molH2发生加成反应。
在一定条件下可发生类似反应①的反应,其产物分子的结构简式为____________;1mol该产物最多可与______molH2发生加成反应。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号