实验室用浓盐酸和MnO2制取并探究Cl2化学性质,装置图下图所示: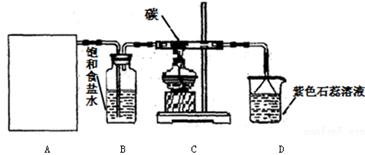
(1)A是氯气发生装置,实验室制取Cl2的原理是 (用化学方程式表示)
(2)该实验中A部分的装置是 (填字母)
(3)从C装置出来的气体中含有CO2和HCl,则从B装置导出的气体成分是 。
(4)D装置的作用是 ,可能观察到的现象是 。
(5)为进行有关氯气的性质实验,需要4瓶容积为122 mL的氯气(室温下,氯气的密度为2.91g/L),理论上需要MnO2的质量是 ,实际称量的MnO2固体的质量必须适当多余理论量,原因是
(6)若将装置A如图所示进行连接,探究其与某些溶液分反应的性质,回答下列问题。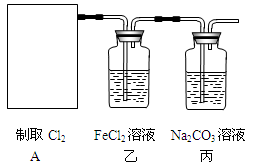
①乙装置中FeCl2溶液与Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是 。
②丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。该物质可能是 。
| A.Cl2 | B.NaClO | C.Na2CO3 | D.Na2O2 |
 粤公网安备 44130202000953号
粤公网安备 44130202000953号