下图是a、b两种物质的溶解度曲线,从中可得出一些相关信息。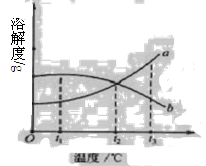
(1)t2℃时,a、b两种物质的溶解度 (填“相等”、“不相等”或“不能确定”).
(2)a、b两种物质一定量的饱和溶液由t2℃升温到t3℃时,溶质质量分数不变的是 。
(3)在t1℃时,60 g水中溶解a物质mg后就不能再溶解了,则溶解a物质mg后形成的溶液属于 溶液(填“饱和”或“不饱和”),其溶质的质量分数为(用含m的计算式表示) .
下图是a、b两种物质的溶解度曲线,从中可得出一些相关信息。
(1)t2℃时,a、b两种物质的溶解度 (填“相等”、“不相等”或“不能确定”).
(2)a、b两种物质一定量的饱和溶液由t2℃升温到t3℃时,溶质质量分数不变的是 。
(3)在t1℃时,60 g水中溶解a物质mg后就不能再溶解了,则溶解a物质mg后形成的溶液属于 溶液(填“饱和”或“不饱和”),其溶质的质量分数为(用含m的计算式表示) .