碳酸钠和碳酸氢钠是生活中常见的两种白色固体。同学们对鉴别这两种物质非常感兴趣,
进行如下探究。
【查阅资料】
1.碳酸钠和碳酸氢钠在不同温度下的溶解度
| |
10℃ |
20℃ |
30℃ |
40℃ |
| Na2CO3 |
12.5 g |
21.5 g |
39.7 g |
49.0 g |
| NaHCO3 |
8.1 g |
9.6 g |
11.1 g |
12.7 g |
2.碳酸钠和碳酸氢钠化学性质(部分)的比较
| 性质 |
Na2CO3 |
NaHCO3 |
性质比较 |
| 溶液的酸碱性 |
碱性 |
碱性 |
相同条件下,Na2CO3溶液的碱性更强 |
| 热稳定性 |
稳定 |
不稳定 |
NaHCO3受热分解生成Na2CO3、CO2和H2O |
| 与盐酸反应 |
反应 |
反应 |
均产生CO2,但NaHCO3与盐酸的反应更加剧烈 |
【设计方案并实施】
| 实验方案 |
实验现象及结论 |
| 方案一:___________ |
若有白色固体剩余,样品为碳酸氢钠;否则为碳酸钠。 |
| 方案二:分别将两种白色固体溶于水制成5%的溶液,___________,将其与标准比色板对照。 |
pH值大的为碳酸钠溶液,pH值小的为碳酸氢钠溶液。 |
| 方案三:分别取少量固体于试管中加 热,然后将产生的气体通入石灰水中。 |
____________ |
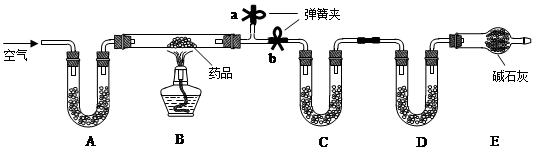
方案四:如下图所示,分别将气球中的固体粉末全部且同时倒入装有过量盐酸的试管中,观察现象。 |
___________________________ |
【实验反思】
通过上述实验,我们知道根据物质的性质设计并进行______实验,能帮助我们更好地理解和掌握相关物质的性质。




 粤公网安备 44130202000953号
粤公网安备 44130202000953号