按下列要求写出由第二周期非金属元素组成的中性分子的相关内容:
(1)平面三角形分子:分子式 ,中心原子杂化方式是 .
(2)三角锥形分子:分子式 ,VSEPR模型的名称为 .
(3)正四面体形分子:结构式
(4)与O22+互为等电子体的一种化合物的分子式为 ,O22+的电子式可表示为_____,1mol O22+ 中含有的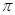 键数目为_____。
键数目为_____。
按下列要求写出由第二周期非金属元素组成的中性分子的相关内容:
(1)平面三角形分子:分子式 ,中心原子杂化方式是 .
(2)三角锥形分子:分子式 ,VSEPR模型的名称为 .
(3)正四面体形分子:结构式
(4)与O22+互为等电子体的一种化合物的分子式为 ,O22+的电子式可表示为_____,1mol O22+ 中含有的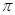 键数目为_____。
键数目为_____。