(每空2分,共8分)下图是某课外学习小组设计的气体制备与性质验证的组合实验,其中装置C的作用是将二氧化碳和炭粉在高温下转化为一氧化碳。请看图回答下列问题: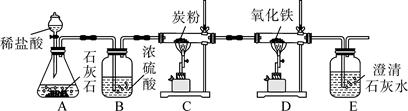
(1)写出装置A中发生反应的化学方程式____________。
(2)装置B中浓硫酸的作用是_____________。
(3)装置D中玻璃管内的实验现象为_____________。
(4)该套装置中有一个明显的不足之处,应在装置E后放置燃着的酒精灯处理尾气。这样做的原因是 。
(每空2分,共8分)下图是某课外学习小组设计的气体制备与性质验证的组合实验,其中装置C的作用是将二氧化碳和炭粉在高温下转化为一氧化碳。请看图回答下列问题:
(1)写出装置A中发生反应的化学方程式____________。
(2)装置B中浓硫酸的作用是_____________。
(3)装置D中玻璃管内的实验现象为_____________。
(4)该套装置中有一个明显的不足之处,应在装置E后放置燃着的酒精灯处理尾气。这样做的原因是 。