[化学——选修3:物质结构与性质](15分)A、B、C、D、E代表五种常见元素,它们的核电荷数依次增大。其中元素E的基态3d轨道上有2个电子,A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素, D与C可形成CD型离子化合物。请回答下列问题:
(1)E的基态原子价层电子排布式为 。
(2)AB2分子中,A的杂化类型为 ;在元素周期表中A、B及与两者紧邻的元素的第一电离能由大到小的顺序为(用元素符号表示) ;1个AB2分子中,含有 个∏键和 个δ键。
(3)AB2形成的晶体的熔点 (填“高于”“低于”或“无法判断”)CD形成的晶体的熔点,原因是 .
(4)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为 (用元素符号表示)。 ED4是制取航天航空工业材料的重要原料。取上述橙红色晶体,放在电炉中,通入D2和A的单质后高温加热,可制得ED4,同时产生一种造成温室效应的气体,写出反应的化学方程式: .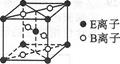
(5)由C、D两元素形成的化合物组成的晶体中,阴、阳离子都具有或近似具有球型对称结构,它们都可以看作刚性圆球,并彼此“相切”。如下图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:若a=5.6×10-8cm,则该晶体的密度为 g·cm-3。(精确到小数点后1位)。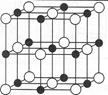
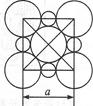
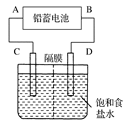
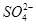 -2e-===PbSO4
-2e-===PbSO4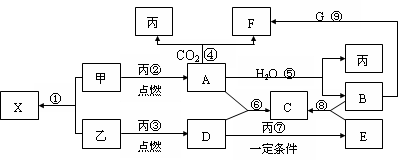
 粤公网安备 44130202000953号
粤公网安备 44130202000953号