工业上用辉铜矿(主要成分Cu2S,含Fe3O4、SiO2杂质)为原料,生产硫酸铜晶体的工艺流程如下: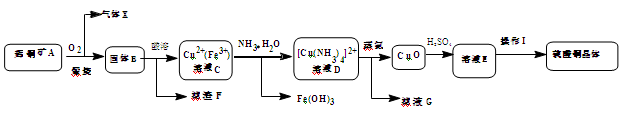
已知:①固体B为氧化物组成的混合物 ②[Cu(NH3)4]2+(aq)  Cu2+(aq) + 4NH3(aq)
Cu2+(aq) + 4NH3(aq)
(1)气体X是 ,高温下在过量空气中煅烧辉铜矿时,Cu2S发生反应的方程式为: 。
(2)固体B酸溶时加入稀硫酸和H2O2,目的是 ,不用浓硫酸的原因是 。
(3)鉴别溶液D中Fe3+完全除尽的方法是 。滤液G的主要溶质是 (填化学式)。
(4)由溶液E获得硫酸铜晶体的实验操作I的方法是蒸发浓缩、降温结晶、 、烘干。
(5)用“间接碘量法”测定所制备的CuSO4·5H2O(不含能与I-反应的氧化性杂质)的纯度。取a g试样配成100 mL溶液,取25.00 mL该溶液,滴加KI溶液后有白色碘化物沉淀生成,滴加KI溶液至沉淀不再产生为止,然后用硫代硫酸钠标准溶液滴定生成的I2,发生反应的化学方程式为I2+2Na2S2O3===2NaI+Na2S4O6,消耗c mol·L-1 Na2S2O3溶液的体积为V mL。
①写出CuSO4与KI反应的离子方程式_________________________。
②计算试样中CuSO4·5H2O的纯度____________________(用a、c、V表示)。
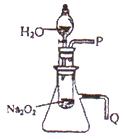

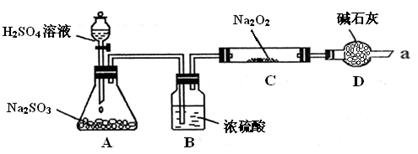

 再加热一定时间,放入干燥器中冷却至室温后称量。重复本操作,直至两次称量结果不变;
再加热一定时间,放入干燥器中冷却至室温后称量。重复本操作,直至两次称量结果不变; 粤公网安备 44130202000953号
粤公网安备 44130202000953号