(本题共10分)
利用镁和稀硫酸反应,不仅可以测定1mol氢气的体积,装置如下左图,也可以测定镁带中镁的质量分数(杂质与酸反应不产生气体),装置如下右图。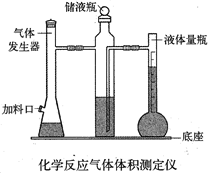
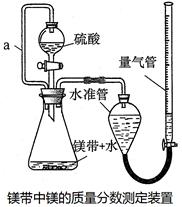
32.用离子方程式表示测定实验的反应原理 。
(本题共10分)
利用镁和稀硫酸反应,不仅可以测定1mol氢气的体积,装置如下左图,也可以测定镁带中镁的质量分数(杂质与酸反应不产生气体),装置如下右图。

32.用离子方程式表示测定实验的反应原理 。