实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如右图所示: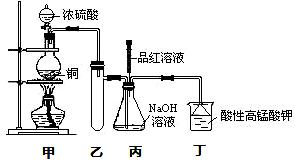
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,则H2SO4是否有剩余________(填“是”或“否”),原因是_______________。
(2)装置乙的作用是_____________________________________________。
(3)装置丁的作用是吸收污染空气的SO2气体,其反应的离子方程为 。
(4)若将SO2 通入氯水中,化学反应方程式为 。
(5)下列说法正确的是________(填序号)。
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
c.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
d.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
(6)现有可供选择的仪器和试剂:烧杯、试管、玻璃棒、胶头滴管; 2 mol/L盐酸、2 mol/L硝酸、1 mol/L氯化钡溶液、l mol/L氢氧化钡溶液、品红溶液、蒸馏水。
请设计实验探究吸收后产物中是否存在NaHSO3 和Na2SO3,将实验操作、预期的实验现象和结论填在下表中。
| 实验操作 |
预期现象与结论 |
| 步骤1:取少量待测液放入试管中,滴加过量l mol/L氯化钡溶液。静置一段时间后,得到滤液A和固体B。 |
|
| 步骤2:往固体B中加入蒸馏水洗涤沉淀,静置后弃去上层清液,向固体滴入2滴品红,再 |
若品红褪色(或有气泡),则 |
| 步骤3: |
若 , 则 ; 否则 。 |

 粤公网安备 44130202000953号
粤公网安备 44130202000953号