铝是自然界中含量最高的金属元素,以铝土矿(主要成分为Al2O3,还含有Fe2O3)为原料通过以下途径制备氯化铝晶体和绿矾晶体:
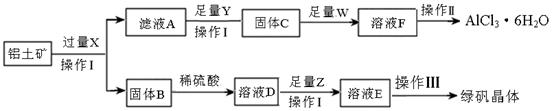
(1)X是__________,操作I是_______。
(2)Z是_____,检验溶液E中含有金属阳离子的实验方法是_______________________。
(3)操作Ⅱ的主要实验步骤是边滴加____(填试剂名称)边蒸发浓缩、冷却结晶、过滤、洗涤。
(4)真空碳热还原—氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)=6AlCl(g)+6CO(g) △H=a kJ·mol-1
3AlCl(g) =2Al(l)+AlCl3(g) △H=b kJ·mol-1
反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H= kJ·mol-1(用含a、b的代数式表示);
(5)铝电池性能优越,海洋灯塔电池是利用铝、石墨为电极材料,海水为电解质溶液,构成电池的其正极反应式为_______________________________;与铅蓄电池相比.释放相同电量时,所消耗金属电极材料的质量比m(Al):m(Pb)=____________。
(6)测定绿矾产品中Fe2+含量的实验步骤:
a.称取5.7g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01mol•L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积为40mL(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)。
①计算上述产品中FeSO4•7H2O的质量分数为________;
②若用上述方法测定的产品中FeSO4•7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有___________(只回答一条即可)。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号