从某些性质看,NH3和H2O,NH4+和H3O+,OH-和NH2-,N3-和O2-两两相当,据此判断下列反应方程式正确的是
①2Na + 2NH3 2NaNH2 + H2↑ ②CaO + 2NH4Cl
2NaNH2 + H2↑ ②CaO + 2NH4Cl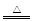 CaCl2 + 2NH3↑+ H2O
CaCl2 + 2NH3↑+ H2O
③3Mg(NH2)2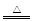 Mg3N2 + 4NH3↑ ④NH4Cl + NaNH2
Mg3N2 + 4NH3↑ ④NH4Cl + NaNH2 NaCl + 2NH3(l)
NaCl + 2NH3(l)
| A.仅①正确 | B.②④正确 | C.全部正确 | D.①②④正确 |
从某些性质看,NH3和H2O,NH4+和H3O+,OH-和NH2-,N3-和O2-两两相当,据此判断下列反应方程式正确的是
①2Na + 2NH3 2NaNH2 + H2↑ ②CaO + 2NH4Cl
2NaNH2 + H2↑ ②CaO + 2NH4Cl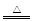 CaCl2 + 2NH3↑+ H2O
CaCl2 + 2NH3↑+ H2O
③3Mg(NH2)2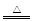 Mg3N2 + 4NH3↑ ④NH4Cl + NaNH2
Mg3N2 + 4NH3↑ ④NH4Cl + NaNH2 NaCl + 2NH3(l)
NaCl + 2NH3(l)
| A.仅①正确 | B.②④正确 | C.全部正确 | D.①②④正确 |