工业上将煤气化过程中生成的CO和H2在一定条件下反应制得甲醇,反应的方程式为:CO(g)+2H2(g) CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
(1)从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2) =____ ;平衡时CO的转化率为____ 。
(2)该反应的平衡常数表达式为 ;若升高反应温度,该反应的平衡常数将 (填“增大”、“减小”或“不变”)。
(3)若在一定温度下,向一恒压容器中充人1 mol CO、2mol H2和1 mol CH3OH,反应达到平衡时,测得混合气体的密度是同温同压下起始混合气体密度的0.8倍,则到达平衡状态前该反应向____ (填“正”或“逆”)反应方向进行。
(4)根据图二,甲醇分解的热化学方程式为 。
(5)若以甲醇为原料制成燃料电池,在碱性介质中负极的电极反应式为____ 。
 碱溶液并微热,则放出能使湿润的红色石蕊试纸变蓝的气体;另取原溶液加入稀H2SO4有气体放出。据此分析该溶液中一定有 、 ;可能有 ;一定没有 ;若要确定可能有的物质可通过 确定(填操作名称)。
碱溶液并微热,则放出能使湿润的红色石蕊试纸变蓝的气体;另取原溶液加入稀H2SO4有气体放出。据此分析该溶液中一定有 、 ;可能有 ;一定没有 ;若要确定可能有的物质可通过 确定(填操作名称)。 ____
____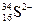 微粒中的质子数是_______,中子数是______
微粒中的质子数是_______,中子数是______ _,核外电子数是_______。
_,核外电子数是_______。 浸取炉渣,过滤.
浸取炉渣,过滤. 3) _____mL,配制用到的仪器有烧杯、玻璃棒、量筒、胶头滴管、 。
3) _____mL,配制用到的仪器有烧杯、玻璃棒、量筒、胶头滴管、 。 粤公网安备 44130202000953号
粤公网安备 44130202000953号