(17分)氢气和氨气都属于无碳清洁能源。
(1)某些合金可用于储存氢,金属储氢的原理可表示为:M(s)+xH2 MH2x(s) △H<0(M表示某种合金)
MH2x(s) △H<0(M表示某种合金)
下图表示温度分别为T1、T2时,最大吸氢量与氢气压强的关系。则下列说法中,正确的是______
| A.T1>T2 |
| B.增大氢气压强,加快氢气的吸收速率 |
| C.增大M的量,上述平衡向右移动 |
| D.在恒温、恒容容器中,达平衡后充入H2,再次平衡后的压强增大 |
(2)以熔融碳酸盐为电解质,稀土金属材料为电极组成氢氧燃料电池(如装置甲所示),其中负极通入H2,正极通入O2和CO2的混合气体。乙装置中a、b为石墨电极,电解过程中,b极质量增加。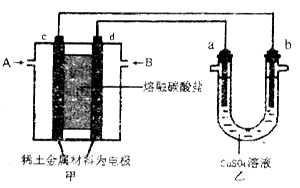
①工作过程中,甲装置中d电极上的电极反应式为____________________。
②若用该装置电解精炼铜,则b极接____(填“粗铜”或“精铜”);若用该装置给铁制品上镀铜,则____(填“a”或“b”)极可用惰性电极(如Pt电极),若电镀量较大,需要经常补充或更换的是_______。
(3)氨在氧气中燃烧,生成水和一种空气组成成分的单质。
已知:①N2(g)十3H2(g)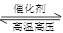 2NH3(g) △H=
2NH3(g) △H=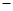 92.4kJ·mol-1
92.4kJ·mol-1
②2H2(g)十O2(g)=2H2O(1) △H=-572KJ·mo1-1
试写出氨气在氧气中燃烧生成液态水的热化学方程式___________________。
(4)在一定条件下,将lmolN2和3molH2混台于一个10L的密闭容器中发生反应:
N2(g)+3H2(g)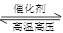 2NH3(g)
2NH3(g)
5min后达到平衡,平衡时氮气的转化率为a。
①该反应的平衡常数K=________,(用含a的代数式表示)
②从反应开始到平衡时N2的消耗速率v(N2)=____mo1·L-1·min-1。(用含a的代数式表示)
 请回答:
请回答:
 表示的分子式;名称是。
表示的分子式;名称是。 中含有的官能团的名称为。
中含有的官能团的名称为。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号