某同学设计如下实验方案,分离KCl和BaCl2两种固体混合物。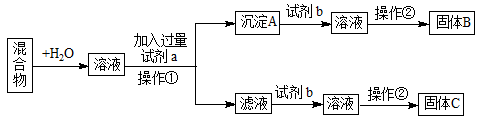
试回答下列问题:
(1)试剂a是 ;试剂b是 ;固体B是 。(填化学式)
(2)操作②的名称是: 、 、干燥。
(3)加入试剂a所发生的离子方程式为: 。
沉淀A与试剂b所发生的离子方程式为: 。
某同学设计如下实验方案,分离KCl和BaCl2两种固体混合物。
试回答下列问题:
(1)试剂a是 ;试剂b是 ;固体B是 。(填化学式)
(2)操作②的名称是: 、 、干燥。
(3)加入试剂a所发生的离子方程式为: 。
沉淀A与试剂b所发生的离子方程式为: 。