下表是元素周期表的一部分,表中的每个字母代表一种短周期元素,回答下列问题: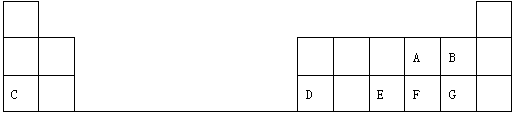
(1)画出A的原子结构示意图________________________。
(2)A、B、E、F、G形成的气态氢化物中最稳定的是_____________(填化学式)。
(3)D在元素周期表中的位置是第3周期 族。
(4)E、F的最高价氧化物对应水化物的酸性,较强的是______________(用化学式表示)。
下表是元素周期表的一部分,表中的每个字母代表一种短周期元素,回答下列问题:
(1)画出A的原子结构示意图________________________。
(2)A、B、E、F、G形成的气态氢化物中最稳定的是_____________(填化学式)。
(3)D在元素周期表中的位置是第3周期 族。
(4)E、F的最高价氧化物对应水化物的酸性,较强的是______________(用化学式表示)。