科学研究表明,月球上有丰富的He资源,可开发利用作未来的新型能源。
(1)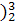 He的中子数是
He的中子数是 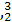 He与
He与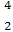 He互称为 。
He互称为 。
(2)α粒子是带有2个单位正电荷、质量数为4的原子核,由此推断α粒子含有 个质子和 个中子。
(3)在 He
He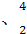 He两种核素中,原子核内的中子数相差为 ,与α粒子有相同质子数和中子数的是 。
He两种核素中,原子核内的中子数相差为 ,与α粒子有相同质子数和中子数的是 。
科学研究表明,月球上有丰富的He资源,可开发利用作未来的新型能源。
(1)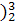 He的中子数是
He的中子数是 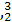 He与
He与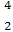 He互称为 。
He互称为 。
(2)α粒子是带有2个单位正电荷、质量数为4的原子核,由此推断α粒子含有 个质子和 个中子。
(3)在 He
He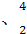 He两种核素中,原子核内的中子数相差为 ,与α粒子有相同质子数和中子数的是 。
He两种核素中,原子核内的中子数相差为 ,与α粒子有相同质子数和中子数的是 。