请根据官能团的不同对下列有机物进行分类
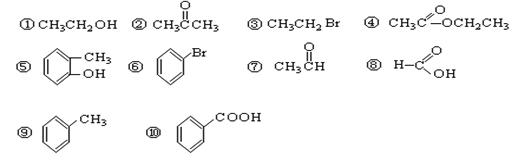
(1)芳香烃: ;(2)卤代烃: ;
(3)醇: ;(4)酚: ;(5)醛: ;
(6)酮: ;(7)羧酸: ;(8)酯: 。
(Ⅱ)
⑴键线式 表示的分子式 。
表示的分子式 。
⑵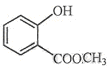 中含有的官能团的名称为 。
中含有的官能团的名称为 。
⑶书写该物质的名称: 
请根据官能团的不同对下列有机物进行分类

(1)芳香烃: ;(2)卤代烃: ;
(3)醇: ;(4)酚: ;(5)醛: ;
(6)酮: ;(7)羧酸: ;(8)酯: 。
(Ⅱ)
⑴键线式 表示的分子式 。
表示的分子式 。
⑵ 中含有的官能团的名称为 。
中含有的官能团的名称为 。
⑶书写该物质的名称: 