有难溶于水的粉末状固体样品,可能含Al、Fe2O3、Cu2O、SiO2、Fe3O4中的一种或几种。
研究小组通过实验确定样品的成分。
查阅资料知:Cu2O + 2H+=Cu + Cu2+ + H2O;
实验步骤:
Ⅰ.取一定量样品于烧杯中,加足量NaOH溶液,有气体产生,过滤得固体A和无色溶液B;
Ⅱ.向B中加入稀硫酸,出现白色沉淀,继续滴加稀硫酸至过量,白色沉淀完全溶解;
Ⅲ.向A中加入足量稀硫酸并微热,固体完全溶解,得溶液C;
Ⅳ.向C中加入NaClO至溶液的pH为4~5,产生红褐色沉淀,过滤得到蓝绿色溶液D;
Ⅴ.向D中加入NaOH至溶液的pH为7~8,产生蓝色絮状沉淀。
请回答下列问题。
(1)Ⅰ中产生气体的离子方程式为 。
(2)由Ⅰ、Ⅱ知,原样品中一定不存在的物质是 。
(3)溶液C中除H+、Cu2+外一定还含有另一种阳离子,为验证存在该阳离子,可选用的试剂为 ,对应的现象是 。
(4)Ⅳ中加NaClO的目的是 。
(5)将Ⅳ中得到的溶液D电解,若电路中有0.1mol电子通过,则理论上阴极质量增重 g。
(6)由上述实验可以获得结论:原样品所有可能的成分组合为组合1: ;组合2: ;组合3: (用化学式表示)








 Cu2++4NH3。请写出在CuSO4溶液中逐滴加入氨水至过量的反应现象: 。
Cu2++4NH3。请写出在CuSO4溶液中逐滴加入氨水至过量的反应现象: 。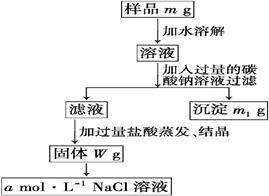
 粤公网安备 44130202000953号
粤公网安备 44130202000953号